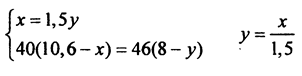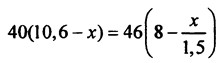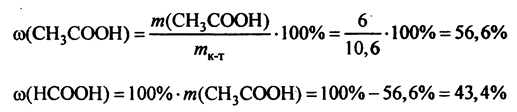Привет. Помогу тебе по самостоялке, чтобы хорошо написал!
1) Рассчитаем содержание гидроксида натрия в растворе:
m (NаОН) = ω (NаОН) ∙mр-ра = 0,04 ∙ 200 = 8 (г)
2) Запишем уравнения реакций нейтрализации уксусной и муравьиной кислот:
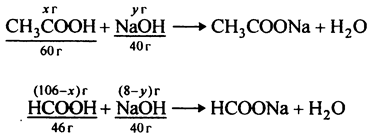
3) Пусть в смеси кислот было х г уксусной кислоты, тогда масса муравьиной кислоты (10,6 - х) г. Пусть на нейтрализацию уксусной кислоты израсходовано у г гидроксида натрия, тогда на нейтрализацию муравьиной кислоты израсходовано (8 - у) г гидроксида натрия. Составим пропорции для расчета масс реагентов в каждой реакции:
60 г СН3СООН — 40 г
NаОН х г СН3СООН — у г
NаОН
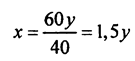
46 г НСООН — 40 г NаОН
(10,6 - х) г НСООН — (8 -у) г NаОН
40 (10,6 — х) = 46 (8 - у)
4) Запишем и решим систему уравнений:
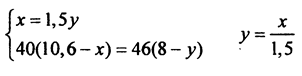
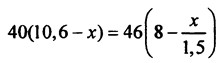
424 - 40 x = 368 - 30,67 x
9,33 x = 56 х = 6
В исходной смеси было 6 г уксусной кислоты.
5) Рассчитаем массовые доли кислот в исходной смеси:
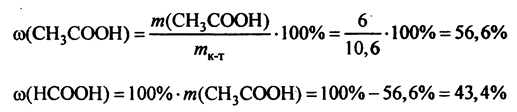
Ответ: 56,6% СН3СООН, 43,4% НСООН.