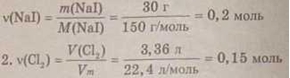Согласно уравнению реакции v(AgNOa) = v(AgCl) → v(AgCl) = 0,1 моль
m(AgCl) = v(AgCl) ∙M(AgCl) =
= 0,1 моль ∙143,5 г/моль = 14,35 г
Ответ: m(AgCl) = 14,35 г 4. 1. m(Nal) = ω(Nal) ∙ m(p-pa) = 0,1 300 г = 30 г
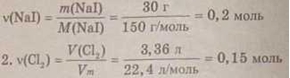
0,2 моль 0,15 моль X моль
3. 2NaI + Cl2 = I2 + 2NaCl
2 моль 1 моль 1 моль
Из уравнения реакции следует, что v(NaI) : v(Cl2) = 2:1, а по условию задачи v(NaI) : v(Cl2) = 0,2 : 0,15, следовательно, хлор дан в избытке, поэтому расчет количества вещества иода проводим по массе иодида натрия,
Согласно уравнению реакции v(NaI) : v(I2) = 2:1→ v(I2) = 0,1 моль