Атом кальция:
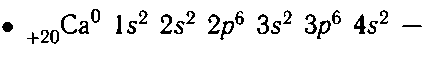
электронная формула атома кальция;
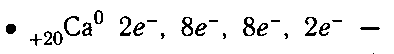
схема строения атома кальция.
Атом кальция отдает внешние 4s2 — электроны,
поэтому химически активен, является щелочнозе-
мельным металлом, взаимодействует с галогенами,
окисляется в сухом воздухе, энергично реагирует
с кислотами, при нагревании взаимодействует с
такими веществами, как F2, S, Н2, N2, С, Р.
Ион кальция:
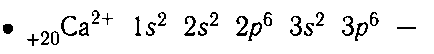
электронная формула иона кальция;
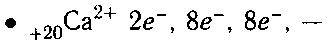
схема строения иона кальция.
Ион кальция не отдает электроны, поэтому
не окисляется, то есть не является химически
активным.
Атом фтора:
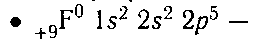
электронная формула атома фтора;
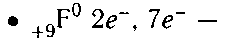
схема строения атома фтора.
Атом фтора может присоединить недостающий
один электрон, является самым активным галоге-
ном, образует соединения практически со всеми
элементами (кроме инертных газов) — фториды,
сильный окислитель и акцептор.
Ион фтора:
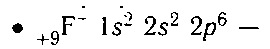
электронная формула иона фтора;
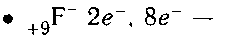
схема строения иона фтора.
Ион фтора не может присоединить электроны,
так как внешняя оболочка иона полностью запол-
нена, входит в состав солей-фторидов.















