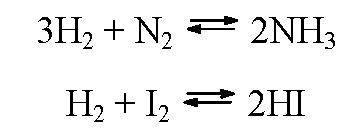Предлагаю вот так написать, должно быть правильно
Химические реакции можно разделить по следующим признакам:
а) По составу исходных веществ и продуктов реакции.
1) Реакции соединения (из нескольких простых или сложных веществ образуется одно сложное)
2Са + O2 = 2СаО
Cu + Сl2 = CuCl2
2) Реакции разложения (из одного сложного вещества образуется несколько простых или сложных)
2Н2О2 = 2H2O + O2
СаСО3 = СаО + СО2
3) Реакции замещения (из простого и сложного вещества образуется простое и сложное)
Zn + СuSО4 = ZnSО4 + Cu
Mg + 2HCl = MgCl2 + H2
4) Реакции обмена (из двух сложных веществ образуется два сложных)
ВаСl2 + NаSО4 = BaSO4↓ + 2NaCl
Рb(NО3)2 + 2КСl = РbСl2↓ + 2KNO3
НNО3 + КОН = КNО3 + Н2О
б) По изменению степени окисления элементов в ходе реакции.
1) Окислительно-восстановительные реакции.
8НNО3 + 3Cu = 3Сu(NО3)2 + 2NO + 4Н2О
2Аl + 6НСl = 2AlCl3 + 3Н2
2) Реакции, в которых степень окисления не изменяется.
2НСl + Са(ОН)2 = СаСl2 + 2Н2О
Na2CO3 + Ва(ОН)2 = ВаСО3↓ + 2NaOH
в) По обратимости.
1) Обратимые (равновесные) реакции.
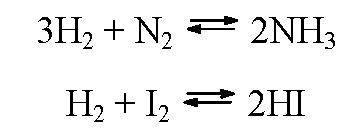
2) Необратимые реакции.
4Mg + 5Н2SО4 = 4MgSО4 + H2S + 4Н2О
НNО3 + КОН = КNО3 + Н2О
г) По тепловому эффекту.
1) Экзотермические реакции (протекающие с выделением
тепла)
2Н2 + О2 = 2Н2О + Q
СН4 + 2О2 = СО2 + 2Н2О + Q
2) Эндотермические реакции (протекающие с поглощением
тепла).
Cu(ОH)2 = CuО + Н2О – Q
H2S = H2 + S – Q