Лабораторный опыт 2 Химия 9 класс Рудзитис, Фельдман. Реакции обмена между растворами электролитов
Реакции обмена между растворами электролитов
Реакции, идущие с образованием осадка. В одну пробирку налейте 3—4 мл раствора сульфата меди(И), во вторую — столько же раствора хлорида кальция, а в третью — сульфата алюминия. В первую пробирку добавьте немного раствора гидроксида натрия, во вторую — раствор ортофосфата натрия, а в третью — раствор нитрата бария. Во всех пробирках образуются осадки.
Задание. Составьте уравнения реакций в молекулярном, ионном и сокращенном ионном виде. Объясните, почему образовались осадки. Растворы каких еще веществ можно прилить в пробирки, чтобы выпали осадки? Составьте уравнения этих реакций в молекулярном, ионном и сокращенном ионном виде.
Реакции, идущие с выделением газа. В одну пробирку налейте 3—4 мл раствора сульфита натрия, во вторую — такой же объем раствора карбоната натрия. В каждую из них добавьте столько же серной кислоты. В первой пробирке выделяется газ с острым запахом, во второй — газ без запаха.
Задание. Составьте уравнения происходящих реакций в молекулярном, ионном и сокращенном ионном виде. Подумайте, какими еще кислотами можно было подействовать на данные растворы, чтобы получить аналогичные результаты. Составьте уравнения этих реакций в молекулярном, ионном и сокращенном ионном виде.
Реакции, идущие с образованием малодиссоциирующего вещества. В одну пробирку налейте 3—4 мл раствора гидроксида натрия и добавьте две-три капли фенолфталеина. Раствор приобретает малиновый цвет. Затем прилейте соляную или серную кислоту до обесцвечивания.
В другую пробирку налейте примерно 10 мл сульфата меди(II) и добавьте немного раствора гидроксида натрия. Образуется голубой осадок гидроксида меди(II). Прилейте в пробирку серную кислоту до растворения осадка.
Задание. Составьте уравнения происходящих реакций в молекулярном, ионном и сокращенном ионном виде. Поясните, почему в первой пробирке произошло обесцвечивание, а во второй — растворение осадка. Каким общим свойством обладают растворимые и нерастворимые основания?
Качественная реакция на хлорид-ион. В одну пробирку налейте 1—2 мл разбавленной соляной кислоты, во вторую — столько же раствора хлорида натрия, а в третью — раствор хлорида кальция. Во все пробирки добавьте по нескольку капель раствора нитрата серебра(I) AgNO3. Проверьте, растворяется ли выпавший осадок в концентрированной азотной кислоте.
Задание. Напишите уравнения соответствующих химических реакций в молекулярном, ионном и сокращенном ионном виде. Подумайте, как можно отличить: а) соляную кислоту от других кислот; б) хлориды от других солей; в) растворы хлоридов от соляной кислоты. Почему вместо раствора нитрата серебра(I) можно также использовать раствор нитрата свинца(II)?
Реакции обмена между растворами электро-
литов
Задание 1.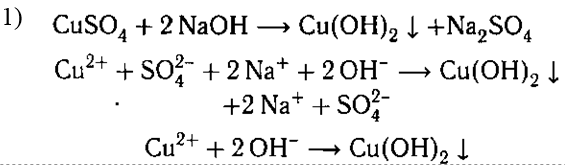
Осадок образуется в результате связывания
ионов Сu2+ и ОН- . Для выпадения осадка из
раствора CuSО4 вместо раствора NaOH можно
взять раствор любой щелочи или растворимых со-
единений бария. Например:
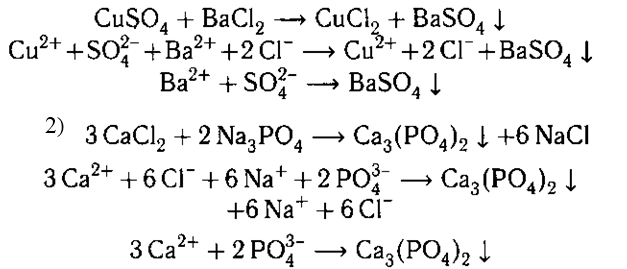
Осадок образуется в результате связывания
ионов Са2+ и РО3-4. Вместо раствора Na3PО4 можно
взять раствор К3РО4 или Н3РО4, а также AgNО3
или Pb(NО3)2. Например: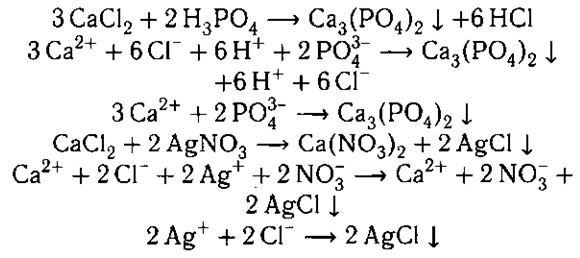
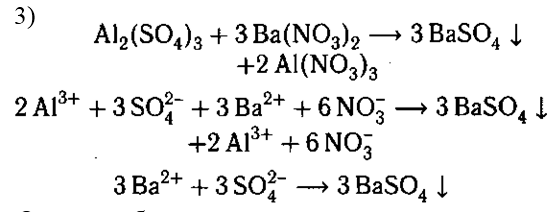
Осадок образуется в результате связывания
ионов Ва2+ и SO42-. Вместо раствора Ba(NО3)2 мож-
но взять любое растворимое соединение бария или
щелочь. Например:
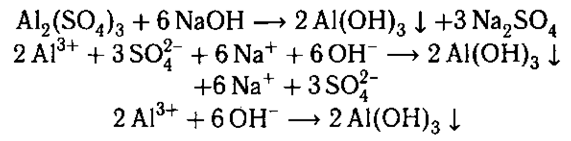
Задание 2.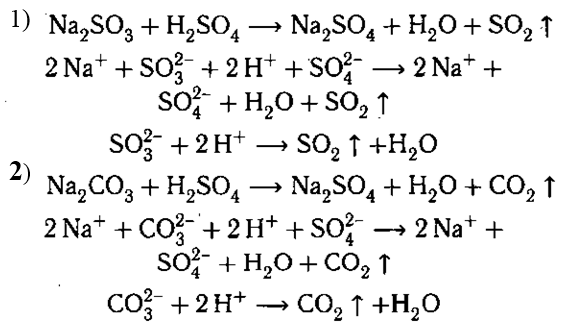
На данные растворы можно было бы подейство-
вать любой более сильной кислотой, например: НСl, HNО3, НВr, Н3РО4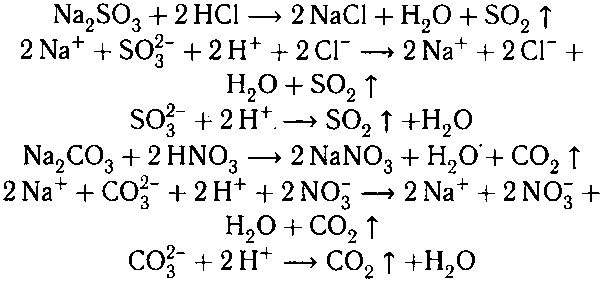
Задание 3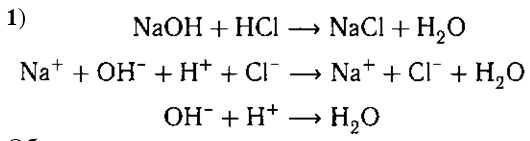
Обесцвечивание произошло за счет того, что фе-
нолфталеин в кислой среде изменяет свою окраску.
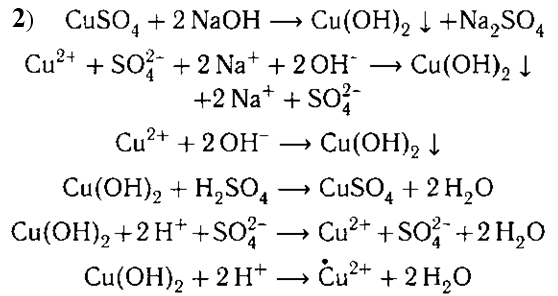
Растворение осадка происходит под действиям
ионов Н+, которые более прочно связаны в случае
воды, чем гидроксида меди (II).
Задание 4
С нитратом свинца также образуется нераство-
римый осадок:
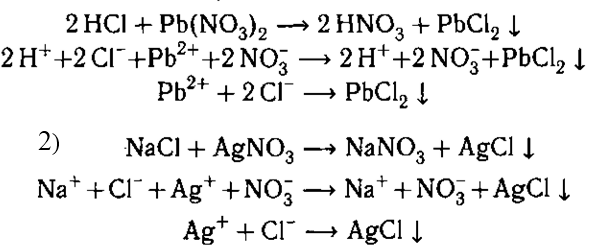
С нитратом свинца также образуется нераство-
римый осадок:
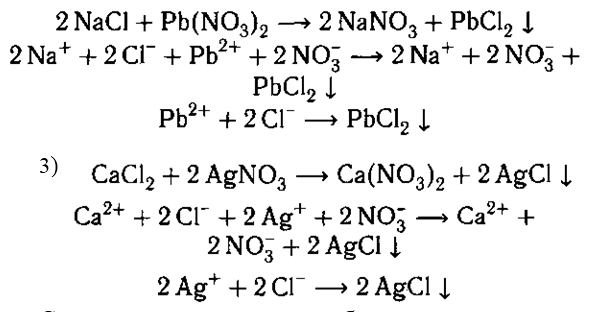
С нитратом свинца также образуется нераство-
римый осадок: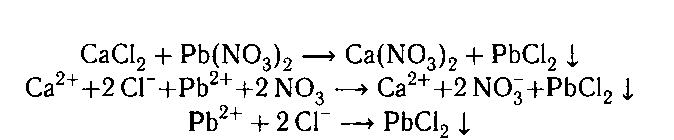
а) и б) Для распознавания соляной кислоты
и ее солей можно использовать раствор нитрата
серебра, так как при их взаимодействии образуется
характерный белый творожистый осадок AgCl, не
растворяющийся даже в концентрированной азот-
ной кислоте. Вместо нитрата серебра можно ис-
пользовать нитрат свинца (II), так как он дает
такую же качественную реакцию с образованием
белого осадка РbСl2.
в) Растворы хлоридов от соляной кислоты можно
отличить с помощью индикатора фенолфталеина,
который в кислой среде приобретает малиновую
окраску.
Подскажите верное решение) вот условие: Какой объем воздуха (н. у.) потребуется для сжигания 1 м3 бутана-1?
Среди предложений 21-29:
(21) И Митрофанов услышал в этом смехе и прощение себе, и даже какое-то (Подробнее...)
16.
Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)
в предложении должна(-ы) стоять запятая(-ые). (Подробнее...)
18.
Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)
в предложении должна(-ы) стоять запятая(-ые). (Подробнее...)















